Trening hipoksyjny w rehabilitacji pacjentów po przebytej chorobie COVID-19
Istnieją również inne niezależne od HIF szlaki sygnalizacyjne, które są aktywowane w warunkach hipoksji, takie jak szlak czynnika jądrowego κB (NF-κB). Dotychczasowe badania wykazały, że czynnik IκBα ulega fosforylacji podczas niedotlenienia, co powoduje jego degradację, a w konsekwencji aktywację NF-κB (1). NF-κB odgrywa kluczową rolę w regulacji odpowiedzi immunologicznej na infekcję. Naukowe opracowania potwierdzają pogląd, że niedotlenienie i stan zapalny mają współzależny związek (2, 3). W rzeczywistości wiele badań wykazuje, że chociaż niedotlenienie może powodować stan zapalny w tkankach, to stabilizacja HIF może hamować stan zapalny i promować procesy regeneracyjne organów (4-7).
Stabilizacja HIF powoduje szeroki zakres odpowiedzi adaptacyjnych, które koncentrują się głównie na regulacji kaskad transkrypcyjnych, które są bardzo ważnym elementem ochrony i procesów adaptacyjnych zachodzących w tkankach. Wiadomo, że HIF-1α (HIF1A) jest związany z aktywacją ekspresji enzymów glikolitycznych, takich jak kinaza fosfoglicerynianowa (PGK) i dehydrogenaza mleczanowa A (LDHA), oba wymagane do metabolicznej adaptacji w sytuacji niewystarczającej ilości tlenu w tkankach, co skutkuje beztlenową produkcją energii w postaci ATP (adenozyno-5′-trifosforan). HIF-2α (HIF2A) indukuje erytropoetynę (EPO) i czynnik wzrostu śródbłonka naczyniowego (VEGF), które pełnią ważną funkcję w angiogenezie, przez co kontrolują prawidłowe rozprowadzanie tlenu w organizmie (8).
Obecnie cykle przerywanej hipoksji (IH – intermittent hypoxia) są podstawą konceptu treningu wysokogórskiego. Jego celem jest poprawienie wydolności tlenowej sportowców lub przyspieszenie reakcji aklimatyzacyjnej na wysokości u alpinistów, poprzez wzrost masy erytrocytów via stymulowanie erytropoezy z udziałem EPO. Pojęcie „treningu w warunkach hipoksji” (HT) powstało już w latach trzydziestych XX wieku i zostało uznane za przydatne narzędzie terapeutyczne po zaobserwowaniu korzystnego wpływu na wiele różnych patologii. Obecnie stosuje się liczne protokoły wykorzystujące ekspozycję na hipoksję w dziedzinie medycyny sportowej w celu poprawy wydolności tlenowej i wstępnej aklimatyzacji do wysokości (9-14).
Fenomen łagodniejszego przebiegu choroby oraz obniżonej ostrości skutków ubocznych po chorobie COVID-19 u osób zamieszkujących obszary wysokogórskie może być związany z procesem adaptacyjnym do niskiego poziomu tlenu, który jest kontrolowany przez czynnik transkrypcyjny HIF-1α.
W minionych latach terapia przerywaną hipoksją, ponad konceptem treningu sportowego, stała się tematem wielu badań naukowych i klinicznych. Stosowanie przerywanej hipoksji (IHT) jako niefarmakologicznej terapii okazało się mieć zdumiewająco pozytywne skutki w przypadku różnych fizjologicznych procesów i schorzeń. Liczne badania wykazały korzystne skutki profilaktyczne, jak i terapeutyczne, użycia metody IHT. Dotychczas wykazano efektywny wpływ terapii przerywaną hipoksją na wiele chorób cywilizacyjnych, takich jak choroby serca, nadwaga, cukrzyca, choroby metaboliczne/mitochondrialne, astma czy choroby neurodegeneracyjne, oraz wpływ IHT na układ odpornościowy i regenerację organów.
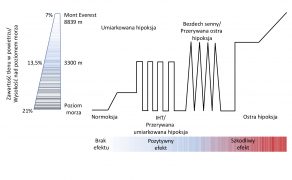
Ogólnie rzecz biorąc, trening hipoksyjny polega na cyklicznej ekspozycji na hipoksję (FiO2 = 10-14%) oraz normoksję (FiO2 = 21%). Cykl może być zindywidualizowany długością ekspozycji na hipoksję oraz normoksję, jednakże ogólnie czas trwania sesji to nie więcej niż 90 minut. Z reguły cała terapia trwa maksymalnie 8 tygodni, a sesje odbywają się od 3 do 7 dni w tygodniu.
Dotychczasowe badania naukowe wykazały bardzo korzystny wpływ terapii hipoksją na stymulowanie procesów regeneracyjnych takich organów jak serce, nerki czy układ nerwowy, które są w szczególności dotknięte powikłaniami po przebytej chorobie COVID-19. Badania przeprowadzone przez grupę naukowców pokazały w modelu mysim, że terapia hipoksją wywołała zainicjowanie procesu regeneracji uszkodzonego mięśnia sercowego, co przejawiało się poprawą ukrwienia i charakterystyką pracy serca, obniżonym poziomem zwłóknienia serca, a tym samym pojawieniem się aktywnych i namnażających się funkcjonalnych komórek mięśnia sercowego (kardiomiocytów) (15). Ponadto kolejne badania pokazały, że zastosowanie terapii hipoksją w modelu szczurzym po indukowanym udarze zwiększyła poziom ekspresji neurotroficznego czynnika pochodzenia mózgowego (BDNF) w uszkodzonych obszarach mózgu, co stymulowało namnażanie się komórek nerwowych, a w konsekwencji obniżenie poziomu uszkodzeń mózgu (16, 17). Do dziś zaprezentowano liczne dodatkowe zastosowania hipoksji w celu stymulacji regeneracji organów, także u człowieka np. badania kliniczne, gdzie zastosowano trening hipoksyjny w ramach rehabilitacji pacjentów z uszkodzonym rdzeniem kręgowym (ClinicalTrials.gov (NCT01272349)).
Mogą zainteresować Cię również
POSTĘPOWANIA
w rehabilitacji